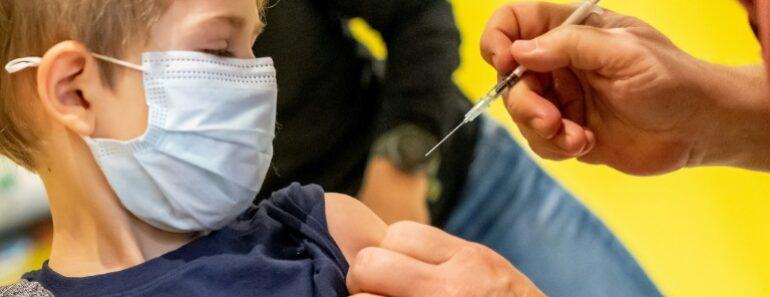
Pfizer-BioNTech reporte sa demande continue à la Food and Drug Administration pour étendre l’utilisation de son vaccin Covid-19 à deux doses pour les enfants âgés de 6 mois à 4 ans.
Cette décision signifie que les vaccins pour ce groupe d’âge ne seront pas disponibles dans les semaines à venir, un revers pour les parents désireux de faire vacciner leurs jeunes enfants.
Pfizer a déclaré vendredi qu’il attendrait ses données sur une série de trois doses du vaccin, car il pense que trois doses « pourraient fournir un niveau de protection plus élevé dans ce groupe d’âge ». Les données sur la troisième dose sont attendues début avril, a indiqué la société.
Pfizer a déclaré en décembre que deux doses n’avaient pas généré une réponse immunitaire suffisamment forte dans son essai sur des enfants âgés de 2 à 4 ans. Pour les jeunes enfants, le vaccin de Pfizer a une dose de 3 microgrammes. Pour les enfants de 5 à 11 ans, la posologie est plus élevée, à 10 microgrammes.
Pourtant, la société a demandé ce mois-ci à la FDA d’autoriser ces deux premières doses, avec un plan pour soumettre des données supplémentaires dans les semaines à venir sur une troisième dose. La série complète de vaccination serait de trois doses.
La FDA devait publier une analyse des données de Pfizer vendredi, avant une réunion du comité consultatif la semaine prochaine. La FDA a déclaré vendredi que la réunion avait été reportée.
Deux personnes familières avec les plans de la FDA ont déclaré qu’il y avait déjà eu beaucoup Pfizer reporte la demande de la FDA pour le vaccin Covid pour les enfants de moins de 5 ans

Pfizer-BioNTech reporte sa demande continue à la Food and Drug Administration pour étendre l’utilisation de son vaccin Covid-19 à deux doses pour les enfants âgés de 6 mois à 4 ans.
Cette décision signifie que les vaccins pour ce groupe d’âge ne seront pas disponibles dans les semaines à venir, un revers pour les parents désireux de faire vacciner leurs jeunes enfants.
Pfizer a déclaré vendredi qu’il attendrait ses données sur une série de trois doses du vaccin, car il pense que trois doses « pourraient fournir un niveau de protection plus élevé dans ce groupe d’âge ». Les données sur la troisième dose sont attendues début avril, a indiqué la société.
Pfizer a déclaré en décembre que deux doses n’avaient pas généré une réponse immunitaire suffisamment forte dans son essai sur des enfants âgés de 2 à 4 ans. Pour les jeunes enfants, le vaccin de Pfizer a une dose de 3 microgrammes. Pour les enfants de 5 à 11 ans, la posologie est plus élevée, à 10 microgrammes.
Pourtant, la société a demandé ce mois-ci à la FDA d’autoriser ces deux premières doses, avec un plan pour soumettre des données supplémentaires dans les semaines à venir sur une troisième dose. La série complète de vaccination serait de trois doses.
La FDA devait publier une analyse des données de Pfizer vendredi, avant une réunion du comité consultatif la semaine prochaine. La FDA a déclaré vendredi que la réunion avait été reportée.
Deux personnes familières avec les plans de la FDA ont estimé qu’il y avait déjà eu beaucoup de refoulement sur l’agence de la part d’experts extérieurs qui craignaient que les données de Pfizer ne soient pas suffisantes. Les experts ont estimé que leurs inquiétudes « tombaient dans l’oreille d’un sourd » au sein de l’agence.
Les régulateurs fédéraux avaient initialement voulu commencer à examiner les données sur deux doses du vaccin tandis que Pfizer continuait de recueillir des données sur un schéma à trois doses.
Les régulateurs pensaient que deux doses fourniraient une protection suffisante – bien que loin d’être idéale – contre la variante omicron du coronavirus alors que les cas pédiatriques augmentaient.
Lancez-vous dans une nouvelle aventure avec DoingBuzz
Découvrez une multitude d'offres d'emploi et de bourses d'études adaptées à votre parcours.
Newsletter
Abonnez-vous et accédez à tous nos articles en premier !